1.电荷守恒规律:电解质溶液中,不论存在多少种离子,溶液总足呈电中性的,即阴离子所带负电荷总数一定等于阳离子所带正电荷总数。如NaHCO3溶液中存在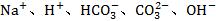 ,则必存在如下关系:
,则必存在如下关系: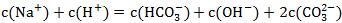 。
。
2.物料守恒规律:电解质溶液中,由于某些离子能够水解而使离子种类增多,但原子总数是守恒的。如K2S溶液中S2-、HS-都能水解,故硫元素以S2-、HS-、H2S三种形式存在,它们之间存在如下关系: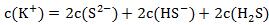 .
.
3.质子守恒规律:质子守恒是指电解质溶液中粒子电离出的H+数等于粒子接受的H+数加游离的H+数。如Na2S水溶液中的质子转移可用图表示如下:
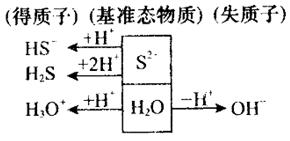
由上图可得Na2S水溶液中质子守恒式可表示为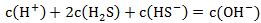 。质子守恒的关系式也可以由电荷守恒与物料守恒推导得到。
。质子守恒的关系式也可以由电荷守恒与物料守恒推导得到。