ֻ��Ҫ����·�QQ���͡��߿���ѧ����ģ�͡����Ϳ��������ȡ���߿���ѧ����ģ�͡��ˣ�
����Һ�е����Ӹ�ˮ�������H+ (��OH-)�������������ʣ��ƻ���ˮ�ĵ���ƽ�⣬�ı�����Һ��H+��OH-�����Ũ�ȣ�ʹ��Һ�ʼ��ԣ������ԣ���
����ˮ��Ĺ��ɣ�˭��˭ˮ�⣬˭ǿ��˭�ԣ���ǿ��ˮ�⣬������ˮ�⣻Խ��Խˮ�⣻ԽϡԽˮ�⣻Խ��Խˮ�⡣
1��ǿ��������ˮ��(��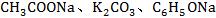 �ȣ���ʵ�������������ˮ�⣬������ˮ�е�H+��ʹOH-��ʣ����Һ�ʼ��ԡ�
�ȣ���ʵ�������������ˮ�⣬������ˮ�е�H+��ʹOH-��ʣ����Һ�ʼ��ԡ�
(1)�ɶ�Ԫ����������γɵ��Σ���ˮ���Ƿֲ��ģ��ҵ�һ��ˮ������Ҫ�ģ��ڶ���ˮ���������Һ���������Ҫȡ���ڵ�һ��ˮ��ij̶ȡ�
(2)��Ԫ�������ʽ������ͬʱ�߱������ˮ�����������е���ˮ��Ϊ������Һ�ʼ��ԣ���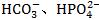 �ȣ����е����Ե���Ϊ������Һ�����ԣ���
�ȣ����е����Ե���Ϊ������Һ�����ԣ���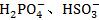 �ȣ���
�ȣ���
2��ǿ��������ˮ��[��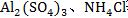 ��]��ʵ��������������ˮ�⣬������ˮ�е�OH-��ʹ��Һ�е�H+��ʣ����Һ�����ԡ�
��]��ʵ��������������ˮ�⣬������ˮ�е�OH-��ʹ��Һ�е�H+��ʣ����Һ�����ԡ�
ע�⣺��Ԫ��������ȻҲ�ֲ�ˮ�⣬�����Ԫ�����������ˮ������Ƚϸ��ӣ���ͨ��������һ�����еģ���Al3+��ˮ�⣬һ��д�ɣ�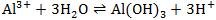 ��
��
3������������(��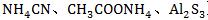 )�������ӽ��ˮ�е�H+�������ӽ��ˮ�е�OH-����ٽ�ˮ�⣬����ˮ��̶Ƚϴ���Һ������������ɵ��������������ǿ���������������ǿ��ʼ��ԣ��������ǿ������ԣ���ǿ���൱����ӽ����ԡ�
)�������ӽ��ˮ�е�H+�������ӽ��ˮ�е�OH-����ٽ�ˮ�⣬����ˮ��̶Ƚϴ���Һ������������ɵ��������������ǿ���������������ǿ��ʼ��ԣ��������ǿ������ԣ���ǿ���൱����ӽ����ԡ�
�������������У���Щ�Σ���Al2S3�ȣ����������ӡ������Ӷ���ˮ�⣬��ˮ���������������������ʻ��ֽ�����ʱ�ε�ˮ�������ܽ��е��ף����������ӷ���ʽӦ�á��T�����ӣ�������������Ҫ���������š�������������š���������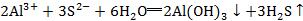 ��
��
 2017�߿����ıر���ʫ��64ƪ���п�Ƭ ��ʫ��������Ĭд�⼰mp3
2017�߿����ıر���ʫ��64ƪ���п�Ƭ ��ʫ��������Ĭд�⼰mp3 �߿���ʷ���Ŀ�����俨Ƭһ���߿�
�߿���ʷ���Ŀ�����俨Ƭһ���߿� �߿�Ӣ��������������ģ����俨Ƭ������и�����������С����Ƭ
�߿�Ӣ��������������ģ����俨Ƭ������и�����������С����Ƭ 2017���´��Ҫ��߿�Ӣ��3500�ʻ㿨Ƭ���������ټDZر��ֲᵥ��
2017���´��Ҫ��߿�Ӣ��3500�ʻ㿨Ƭ���������ټDZر��ֲᵥ�� �и߿���ѧ����ʽ���俨Ƭ���л�ѧ�ر�����ʽ��
�и߿���ѧ����ʽ���俨Ƭ���л�ѧ�ر�����ʽ�� �߿������Ĵ�����ü��俨Ƭ
�߿������Ĵ�����ü��俨Ƭ ���������Ļ���֪ʶ�� �߿�����������֪ʶ���ۿ�Ƭ �߿���������
���������Ļ���֪ʶ�� �߿�����������֪ʶ���ۿ�Ƭ �߿��������� �߿�������ʵ�ʼ��俨Ƭ
�߿�������ʵ�ʼ��俨Ƭ �߿�������ͨ���ּ��俨Ƭ
�߿�������ͨ���ּ��俨Ƭ �߿�������18����ʼ��俨Ƭ
�߿�������18����ʼ��俨Ƭ �߿������ĹŽ�������俨Ƭ
�߿������ĹŽ�������俨Ƭ �߿��������յ�Ӣ�ﵥ�ʶ��│�и߿�Ӣ���Ƶ�����ֲ�߿�����
�߿��������յ�Ӣ�ﵥ�ʶ��│�и߿�Ӣ���Ƶ�����ֲ�߿�����