ֻ��Ҫ����·�QQ���͡��߿���ѧ���Ŀ��㡱���Ϳ��������ȡ���߿���ѧ���Ŀ��㡷�ˣ�
����һ��Ŀ��淴Ӧ��mA(g)+nB(g)⇌ C(g)+qD(g)������һ���¶��´ﵽ��ѧƽ��ʱ���仯ѧƽ�ⳣ�����Ա�ʾΪ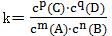 ��
��
(1)���û�ѧƽ�ⳣ�����жϻ�ѧƽ���������¶���ֵ��Kֻ���¶�Ӱ�죬�뷴Ӧ����������Ũ�ȱ仯�ء�����ƽ��״̬�и���ֵ����ʵ���Ũ�ȣ����Լ�������¶��µĻ�ѧƽ�ⳣ���������жϷ�Ӧ�¶ȡ�
(2)���û�ѧƽ�ⳣ�����жϿ��淴Ӧ�Ľ��з���������仯����ѧƽ�ⳣ������˵�����淴Ӧ������Ӧ�����ƶ�����Ϸ�Ӧ�¶ȵı仯�������жϷ�Ӧ�������仯��
(3)���û�ѧƽ�ⳣ�����жϿ��淴Ӧ�Ƿ���ƽ��״̬������ij�¶��¿��淴ӦmA(g)+nB(g)⇌pC(g)+qD(g)��ƽ�ⳣ��ΪK��ijʱ�̷�Ӧ����������Ũ�ȹ�ϵ���£�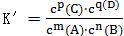 ����K��=K��v(��)=v���棩�����淴Ӧ���ڻ�ѧƽ��״̬����K�䩂K��v(��)��v���棩�����淴Ӧ������Ӧ������У���K�䩃K��v��������v���棩�����淴Ӧ���淴Ӧ������С�
����K��=K��v(��)=v���棩�����淴Ӧ���ڻ�ѧƽ��״̬����K�䩂K��v(��)��v���棩�����淴Ӧ������Ӧ������У���K�䩃K��v��������v���棩�����淴Ӧ���淴Ӧ������С�
(4)���û�ѧƽ�ⳣ�����Խ�����ؼ��㡣����ƽ�⽨����������ֵ����ʵ���Ũ�ȱ仯����ϻ�ѧƽ����������Խ��и���ֵ����ʵ�������Ũ�ȣ���ת���ʵ���ؼ��㡣
ע����Ӱ�컯ѧ��Ӧ���ʵ����أ���һ��Ӱ�컯ѧƽ�⣨���������Ӱ�컯ѧƽ������أ���һ��Ӱ�컯ѧƽ�ⳣ������Ũ�ȡ�ѹǿ����ֻ���¶ȶԶ��߶���Ӱ�졣
 2017�߿����ıر���ʫ��64ƪ���п�Ƭ ��ʫ��������Ĭд�⼰mp3
2017�߿����ıر���ʫ��64ƪ���п�Ƭ ��ʫ��������Ĭд�⼰mp3 �߿���ʷ���Ŀ�����俨Ƭһ���߿�
�߿���ʷ���Ŀ�����俨Ƭһ���߿� �߿�Ӣ��������������ģ����俨Ƭ������и�����������С����Ƭ
�߿�Ӣ��������������ģ����俨Ƭ������и�����������С����Ƭ 2017���´��Ҫ��߿�Ӣ��3500�ʻ㿨Ƭ���������ټDZر��ֲᵥ��
2017���´��Ҫ��߿�Ӣ��3500�ʻ㿨Ƭ���������ټDZر��ֲᵥ�� �и߿���ѧ����ʽ���俨Ƭ���л�ѧ�ر�����ʽ��
�и߿���ѧ����ʽ���俨Ƭ���л�ѧ�ر�����ʽ�� �߿������Ĵ�����ü��俨Ƭ
�߿������Ĵ�����ü��俨Ƭ ���������Ļ���֪ʶ�� �߿�����������֪ʶ���ۿ�Ƭ �߿���������
���������Ļ���֪ʶ�� �߿�����������֪ʶ���ۿ�Ƭ �߿��������� �߿�������ʵ�ʼ��俨Ƭ
�߿�������ʵ�ʼ��俨Ƭ �߿�������ͨ���ּ��俨Ƭ
�߿�������ͨ���ּ��俨Ƭ �߿�������18����ʼ��俨Ƭ
�߿�������18����ʼ��俨Ƭ �߿������ĹŽ�������俨Ƭ
�߿������ĹŽ�������俨Ƭ �߿��������յ�Ӣ�ﵥ�ʶ��│�и߿�Ӣ���Ƶ�����ֲ�߿�����
�߿��������յ�Ӣ�ﵥ�ʶ��│�и߿�Ӣ���Ƶ�����ֲ�߿�����