(1)根据原子结构
电子层数越多、最外层电子数越少,金属性越强,反之越弱。
(2)根据在周期表中的位置
①同周期元素,从左到右,随着原子序数的增加,金属性减弱;
②同主族元素,从上至下,随着原子序数的增加,金属性增强。
(3)根据金属活动性顺序表
金属的位置越靠前,其金属性越强。
(4)根据实验
①根据金属单质与水(或酸)反应的难易程度:越易反应,则对应的金属元素的金属性越强。
②根据金属单质与盐溶液的置换反应:A置换出B,则A对应的金属元素比B对应的金属元素的金属性强。
③根据金属单质的还原性或对应阳离子的氧化性强弱:单质的还原性越强,对应阳离子的氧化性越弱,元素的金属性越强(Fe对应的是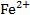 ,而不是
,而不是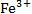 )。
)。
④根据最高价氧化物对应水化物的碱性强弱:碱性越强,则其对应金属元素的金属性越强。
⑤根据电化学原理:不同金属形成原电池时,做负极的金属活泼;在电解池中的惰性电极上,先析出的金属不活泼。