ֻ��Ҫ����·�QQ���͡��߿���ѧ���Ŀ��㡱���Ϳ��������ȡ���߿���ѧ���Ŀ��㡷�ˣ�
(1)һ����
������Һ�л�����ˮ�������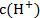 ��
��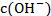 ������pH�Ķ������ù�ʽֱ�Ӽ��㡣
������pH�Ķ������ù�ʽֱ�Ӽ��㡣
(2)ϡ����
����pH=a���ᣬǿ��ʱϡ��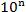 ����pH=a+n������ʱϡ��
����pH=a+n������ʱϡ��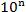 ����a<pH<a+n��
����a<pH<a+n��
����pH=b�ļǿ��ʱϡ��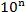 ����pH=b+n������ʱϡ��
����pH=b+n������ʱϡ��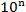 ����b��pH<b-n��
����b��pH<b-n��
(3)�����
��ǿ���ǿ����
��ǿ���Ϻ���Һ�У������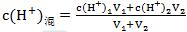 ���������Ϻ��
���������Ϻ��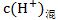 ���ٸ���
���ٸ���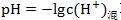 ��pH��
��pH��
��ǿ���ǿ����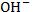
��ǿ���Ϻ���Һ��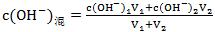 ���������Ϻ��
���������Ϻ��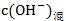 ����ͨ��
����ͨ��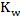 ���
���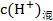 �������pH��
�������pH��
��ǿ���ǿ����
ǿ���ǿ����кͷ�Ӧ������ǿ���ǿ���������ͬ����Ҫ�С���ȫ�͡��͡������͡��������ͣ�ǡ���к͡�ǿ�������ǿ��������������
ǿ��ǿ��ǡ���к�ʱ��ǿ����������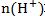 ��ǿ����������
��ǿ����������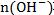 ��ȣ���Ӧ��õ�����ǿ��ǿ���Σ���ҺΪ���ԣ�pH=7��
��ȣ���Ӧ��õ�����ǿ��ǿ���Σ���ҺΪ���ԣ�pH=7��
��ǿ��ʣ��ʱ������Ҫ�����ʣ���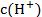 ��Ȼ���ٸ��ݶ��������Һ��pH��
��Ȼ���ٸ��ݶ��������Һ��pH��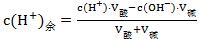 ��
��
��ǿ��ʣ��ʱ������Ҫ�����ʣ���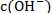 ��Ȼ������ˮ�����ӻ�����������Һ��
��Ȼ������ˮ�����ӻ�����������Һ��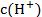 �������ݶ��������Һ��pH��
�������ݶ��������Һ��pH��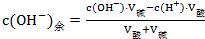 ��
��
 2017�߿����ıر���ʫ��64ƪ���п�Ƭ ��ʫ��������Ĭд�⼰mp3
2017�߿����ıر���ʫ��64ƪ���п�Ƭ ��ʫ��������Ĭд�⼰mp3 �߿���ʷ���Ŀ�����俨Ƭһ���߿�
�߿���ʷ���Ŀ�����俨Ƭһ���߿� �߿�Ӣ��������������ģ����俨Ƭ������и�����������С����Ƭ
�߿�Ӣ��������������ģ����俨Ƭ������и�����������С����Ƭ 2017���´��Ҫ��߿�Ӣ��3500�ʻ㿨Ƭ���������ټDZر��ֲᵥ��
2017���´��Ҫ��߿�Ӣ��3500�ʻ㿨Ƭ���������ټDZر��ֲᵥ�� �и߿���ѧ����ʽ���俨Ƭ���л�ѧ�ر�����ʽ��
�и߿���ѧ����ʽ���俨Ƭ���л�ѧ�ر�����ʽ�� �߿������Ĵ�����ü��俨Ƭ
�߿������Ĵ�����ü��俨Ƭ ���������Ļ���֪ʶ�� �߿�����������֪ʶ���ۿ�Ƭ �߿���������
���������Ļ���֪ʶ�� �߿�����������֪ʶ���ۿ�Ƭ �߿��������� �߿�������ʵ�ʼ��俨Ƭ
�߿�������ʵ�ʼ��俨Ƭ �߿�������ͨ���ּ��俨Ƭ
�߿�������ͨ���ּ��俨Ƭ �߿�������18����ʼ��俨Ƭ
�߿�������18����ʼ��俨Ƭ �߿������ĹŽ�������俨Ƭ
�߿������ĹŽ�������俨Ƭ �߿��������յ�Ӣ�ﵥ�ʶ��│�и߿�Ӣ���Ƶ�����ֲ�߿�����
�߿��������յ�Ӣ�ﵥ�ʶ��│�и߿�Ӣ���Ƶ�����ֲ�߿�����